고객지원
기기원리
시료 용액에 담궈 놓은 지시 전극(Indicator electrode)과 기준 전극(Reference electrode) 사이의 전위차 변화를 측정하여 적정의 당량점을 결정하는 방법입니다. 분 석하려는 성분의 함량 변화에 따라 전위를 변화시켜 주는 지시 전극과 어떤 용액에 담궈도 액간 접촉 전위를 변화시키지 않는 기준 전극을 연결하고 적정액의 전위차 변 화를 측정합니다. 전위차 적정은 중화 적정법,산화환원 적정법,침전 적정법, 착물형성 적정법 등에 이용 가능합니다.
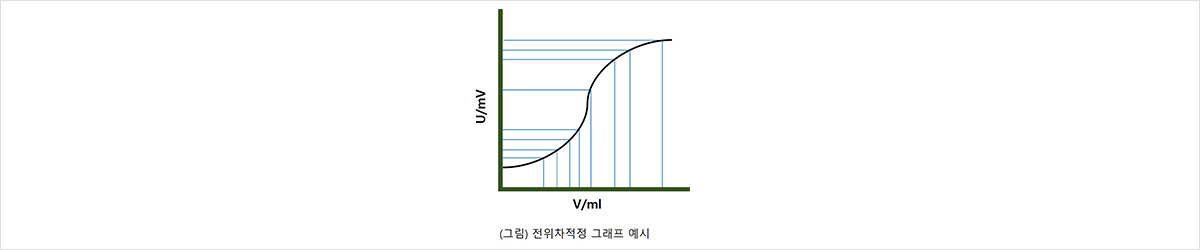
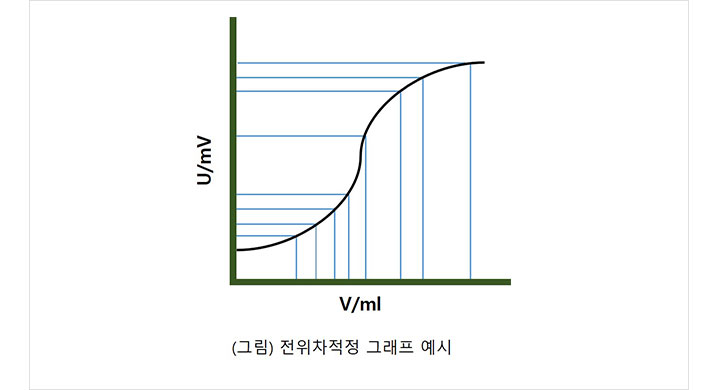
-일반 중화 또는 산화환원적정보다 정밀한 측정이 가능합니다.
- 지시약을 사용하지 않고 정확하게 당량점을 결정할 수 있습니다.
- 분석 결과는 별도의 보정 없이 분석 물질에 대한 정보를 제공합니다.
- 적정은 분석 장비 설치부터 분석 결과 도출까지 빠른 진행이 가능합니다.
- 무기 이온 분석부터 복잡한 유기 혼합물까지 ppm, ppb 범위로 미량 분석이 가능합니다.
- 재현성과 정밀도가 높습니다.
- 다른 분석법에 비해 비용이 저렴합니다
- 다음과 같은 경우에 전위차적정을 적용할 수 있습니다.
-
- 유색 용액의 경우
- 적당한 지시약이 없을 경우
- 유기용매를 사용하는 경우
- 지시약의 색상변화를 뚜렷하게 구별하기 어려운 경우
- 실험자에 따른 개인오차를 줄이는 경우 배제
- 다수의 시료를 분석하는 경우
적정에 의해 시료 중 특정 성분의 함량을 결정하기 위해 이용되는 반응이 어떤 반응인지 확인 후 적절한 적정액과 전극을 선택하여 분석 해야합니다.
- 중화적정(Neutralization Titration)
- 중화적정법은산을 알칼리 표준액으로 정량하는 산적정법(Acidimetry)과 염기를 산 표준액으로 정량하는 염기적정법(Alkalimetry) 2가지로 나누어집니다.산,염 기가 아니라도 Na2CO3, Na2B4O7, NH4OH 등과 같이 수용액에서 가수분해하여 H+, OH- 를 생성하는 물질은 중화적정법으로 분석 가능합니다. 중화반응에서 이용 되는 전극은 시료 용액중 수소 이온의 함량변화를 감지할수 있는 pH 전극을 지시 전극으로 사용합니다.수용성 용매는 복합 pH 전극이 일반적으로 사용되며, 비수 용성 용매는 지시전극과 기준전극이 사용되는데 이 경우 기준전극의 충진액 선택이 고려되어야 합니다.
- 산화환원적정 (Redox Titration)
-
산화환원 적정시 적정 당량점 부근에서 전위가 급변하는 특성과적절한 전극을사용하여 그 반응의 당량점을 결정하는 전위차적정의 한 종류입니다.일반적으로 지 시전극은금속 전극인 Pt(백금), Au(금)를 이용하며, 기준 전극은 Ag/AgCl 전극을 사용합니다.이외에도지시 전극과 기준 전극을 결합한 복합 전극 (Combined ele ctrode)을 수용성 용매에서 측정 시 사용합니다.
산화환원적정은 적정액의 종류에 따라 몇가지로 분류됩니다.
- Cerimetry : Ce4+염인 (NH4)4Ce(SO4)4• 2H2O를 산성액에서 산화제로 사용하여 적정하는 방법
- Manganometry : 강력한 산화제인 KMnO4를 적정액으로 사용하는 방법
- Dichromatometry : 산화제인 K2Cr2O7를 적정액으로 사용하는 방법
- Diazotisation :NaNO2를 적정액으로 사용하여 방향족아민의 정량에 이용되는 적정법
- Iodometry & Iodimetry :I2 표준액을 사용하여 시료를 산화시키거나(Iodimetry) 유리되어나오는 I2 를 Na2S2O3액으로적정하는Iodometry) 방법
- KBrO3, KIO3법 : KBrO3, KIO3 표준액을 사용하여 적정하는 방법
- 침전적정 (Precipitation Titration)
-
가장 대표적인 침전적정은 은이온과할로겐 이온이 반응하여 할로겐화은(Silver Halogenide) 침전을 형성하는 은적정법(Argentometric Titration)입니다. 표준 적정액의Ag+이온이 당량점을 지나 시료용액내에 존재하는 순간 전위가 급격하게 변화하고 지시전극으로 사용되는 Ag전극이 이 변화를 감지합니다.
Ex) Cl- + Ag+ → AgCl (침전)
- 착물형성적정 (Complexometric Titration)
-
금속이온을 정량하는 방법인 착물형성 적정은 금속 이온선택전극(ISE)을지시 전극으로 사용하며, 시료에 포함된 금속이온과 EDTA의 반응에 따른 금속이온 농도 의 변화를 전위값으로나타냅니다. 킬레이트제로서 Cu-EDTA를 사용하는 경우에는 Cu-EDTA가 시료금속 이온과 착물을 모두 형성하고 Cu가시료용액 중에 과잉으 로 존재할 때 변화하는 전위차를 지시 전극인 Cu ISE가 감지합니다. 사용되는 적정액의 종류에 따라 알맞은 전극을 선택해야하며,기준 전극으로 Ag/AgCl 전극을 주로 이용합니다.
Ex) Ca2+ + H2EDTA2- → Ca-EDTA2- + 2H+




 개인정보취급방침
개인정보취급방침